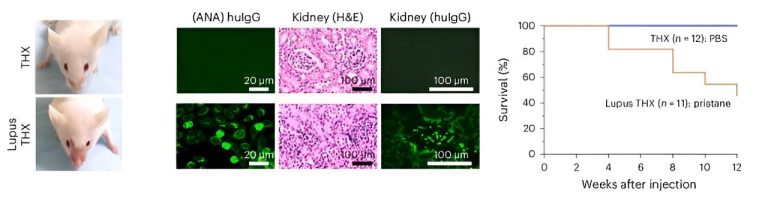
Skuqje malare majtas në një mi Lupus THX (të rrjedhur nga huNSGW41) (tre javë pas injektimit të pristanit). IgG-të e mesme antinukleare të serumit (shiriti i shkallës, 20 μm) dhe imunopatologjia e veshkave (imunofluoreshenca H&E dhe anti-huIgG; shiriti i shkallës, 100 μm) në minjtë Lupus THX dhe THX (12 javë pas injektimit të pristanit ose PBS). Kredia: Imunologjia e Natyrës (2024). DOI: 10.1038/s41590-024-01880-3
Një zbulim i madh për kërkimin biomjekësor premton njohuri të reja në zhvillimin e imunoterapisë dhe modelimin e sëmundjeve. Shkencëtarët në Qendrën e Shkencave Shëndetësore të Universitetit të Teksasit në San Antonio kanë krijuar një model të humanizuar miu me një sistem imunitar të njeriut dhe një mikrobiom të zorrëve të ngjashme me njeriun, i cili është i aftë të krijojë përgjigje specifike të antitrupave.
Shkencëtarët u drejtuan nga Paolo Casali, MD, profesor i Universitetit të Teksasit Ashbel Smith dhe profesor i shquar i kërkimit, Departamenti i Mikrobiologjisë, Imunologjisë dhe Gjenetikës Molekulare në Shkollën e Mjekësisë Joe R. dhe Teresa Lozano Long. Casali ka pesë dekada përvojë kërkimore biomjekësore në imunologji dhe mikrobiologji dhe është një studiues kryesor në gjenetikën molekulare dhe epigjenetikën e përgjigjes së antitrupave.
Qëllimi i projektit shumëvjeçar, i cili shfaqet në numrin e gushtit 2024 të Imunologjia e Natyrësishte për të kapërcyer kufizimet e modeleve njerëzore aktualisht të disponueshme in vivo duke krijuar një mi të humanizuar me një sistem imunitar të njeriut plotësisht të zhvilluar dhe funksional.
Minjtë përdoren gjerësisht në kërkimet biologjike dhe biomjekësore sepse janë të vegjël, të lehtë për t’u trajtuar, ndajnë shumë elementë imunitarë dhe veti biologjike me njerëzit dhe modifikohen lehtësisht gjenetikisht.
Megjithatë, shumë prej më shumë se 1600 gjeneve të përgjigjes imune të miut nuk janë në përputhje me ekuivalentët e tyre njerëzorë, duke rezultuar në divergjenca ose mangësi të minjve si parashikues të përgjigjeve imune njerëzore. Kjo bëri që disponueshmëria e një modeli të “humanizuar” të miut që riprodhon me besnikëri përgjigjet imune njerëzore të jetë një prioritet i lartë.
Minjtë e parë të humanizuar u krijuan në vitet 1980 për të modeluar infeksionin e njeriut me HIV dhe përgjigjen imune të njeriut ndaj HIV. Minjtë e humanizuar u krijuan dhe janë krijuar që atëherë, duke injektuar minj me mungesë imuniteti me limfocite periferike njerëzore, qeliza burimore hematopoietike ose qeliza të tjera njerëzore.
Modelet e mëparshme dhe ato aktuale, megjithatë, nuk zhvillojnë një sistem imunitar të njeriut plotësisht funksional, kanë një jetëgjatësi të shkurtër dhe nuk krijojnë përgjigje efikase imune. Kjo i bën ato të papërshtatshme për zhvillimin e imunoterapive njerëzore in vivo, modelimin e sëmundjeve njerëzore ose zhvillimin e vaksinave njerëzore.
Ekipi i Casali filloi me injektimin e minjve mutant NSG W41 me imunitet të pamjaftueshëm në mënyrë intrakardiake (barkushe të majtë) me qeliza burimore njerëzore që ata pastruan nga gjaku i kordonit kërthizor.
Pas disa javësh, pasi të jetë vendosur grafti, minjtë kushtëzohen hormonalisht me 17b-estradiol (E2), forma më e fuqishme dhe e bollshme e estrogjenit në trup. Kushtëzimi hormonal nga estrogjeni u nxit nga kërkimet e mëparshme nga Casali dhe të tjerë që sugjeronin se estrogjeni rrit mbijetesën e qelizave burimore njerëzore, nxit diferencimin e limfociteve B dhe prodhimin e antitrupave ndaj viruseve dhe baktereve.
Minjtë e humanizuar që rezultojnë, të quajtur TruHuX (për njeriun e vërtetë, ose THX), zotërojnë një sistem imunitar të njeriut plotësisht të zhvilluar dhe plotësisht funksional, duke përfshirë nyjet limfatike, qendrat germinale, qelizat epiteliale të timusit, limfocitet T dhe B të njeriut, limfocitet B të kujtesës, dhe qelizat plazmatike që prodhojnë antitrupa dhe autoantitrupa shumë specifikë identikë me ato të njerëzve.
Minjtë THX montojnë përgjigje të pjekura të antitrupave neutralizues ndaj Salmonella Typhimurium dhe virusit SARS-CoV-2 Spike S1 RBD pas vaksinimit me Salmonella flagellin dhe vaksinën Pfizer COVID-19 mRNA, përkatësisht. Minjtë THX janë gjithashtu të prirur për të zhvilluar autoimunitet të plotë sistemik lupus pas një injeksioni të pristanit, një vaj që shkakton një përgjigje inflamatore.
Casali tha se zbulimi i miut THX hap mundësitë për eksperimentimin in vivo të njeriut, për zhvillimin e imunoterapeutikëve si frenuesit e pikave të kontrollit të kancerit, zhvillimin e vaksinave njerëzore bakteriale dhe virale, si dhe modelimin e shumë sëmundjeve njerëzore. Ai gjithashtu shpreson se qasja e re mund ta bëjë të vjetëruar përdorimin e primatëve jo-njerëzor për kërkime biomjekësore imunologjike dhe mikrobiologjike.
Meqenëse kërkimet e mëparshme mbi efektin e estrogjenit dhe sistemit imunitar janë të pakta, Casali shpreson që ky zbulim të nxisë kërkime të mëtejshme në këtë temë.
“Duke shfrytëzuar në mënyrë kritike aktivitetin e estrogjenit për të mbështetur diferencimin e qelizave burimore njerëzore dhe qelizave imune njerëzore dhe përgjigjet e antitrupave, minjtë THX ofrojnë një platformë për studimet e sistemit imunitar të njeriut, zhvillimin e vaksinave njerëzore dhe testimin e terapisë,” tha Casali.
Me modelin THX, laboratori Casali tani po heton përgjigjen imune njerëzore in vivo ndaj SARS-CoV-2 (COVID-19) në nivelet sistematike dhe lokale, dhe limfocitet B të kujtesës njerëzore, varësinë nga receptori bërthamor RORα për gjenerimin e tyre. dhe ngjarjet që çojnë në shprehjen dhe disrregullimin e RORα.
Ata po eksplorojnë gjithashtu faktorët dhe mekanizmat epigjenetikë që ndërmjetësojnë gjenerimin e qelizave plazmatike njerëzore, fabrikat e qelizave që prodhojnë antitrupa – fjalë për fjalë mijëra në sekondë – ndaj baktereve, viruseve ose qelizave kancerogjene.
Më shumë informacion:
Daniel P. Chupp et al, Një mi i humanizuar që monton reagime të pjekura të antitrupave të ndërruara, të hipermutuara dhe neutralizuese, Imunologjia e Natyrës (2024). DOI: 10.1038/s41590-024-01880-3
Siguruar nga Qendra e Shkencave Shëndetësore e Universitetit të Teksasit në San Antonio
Citim: Shkencëtarët krijojnë modelin e parë të miut me sistem imunitar të plotë, funksional të njeriut (2024, 8 korrik) marrë më 8 korrik 2024 nga https://medicalxpress.com/news/2024-07-scientists-mouse-functional-human-immune.html
Ky dokument i nënshtrohet të drejtës së autorit. Përveç çdo marrëveshjeje të drejtë për qëllime studimi ose kërkimi privat, asnjë pjesë nuk mund të riprodhohet pa lejen me shkrim. Përmbajtja ofrohet vetëm për qëllime informative.